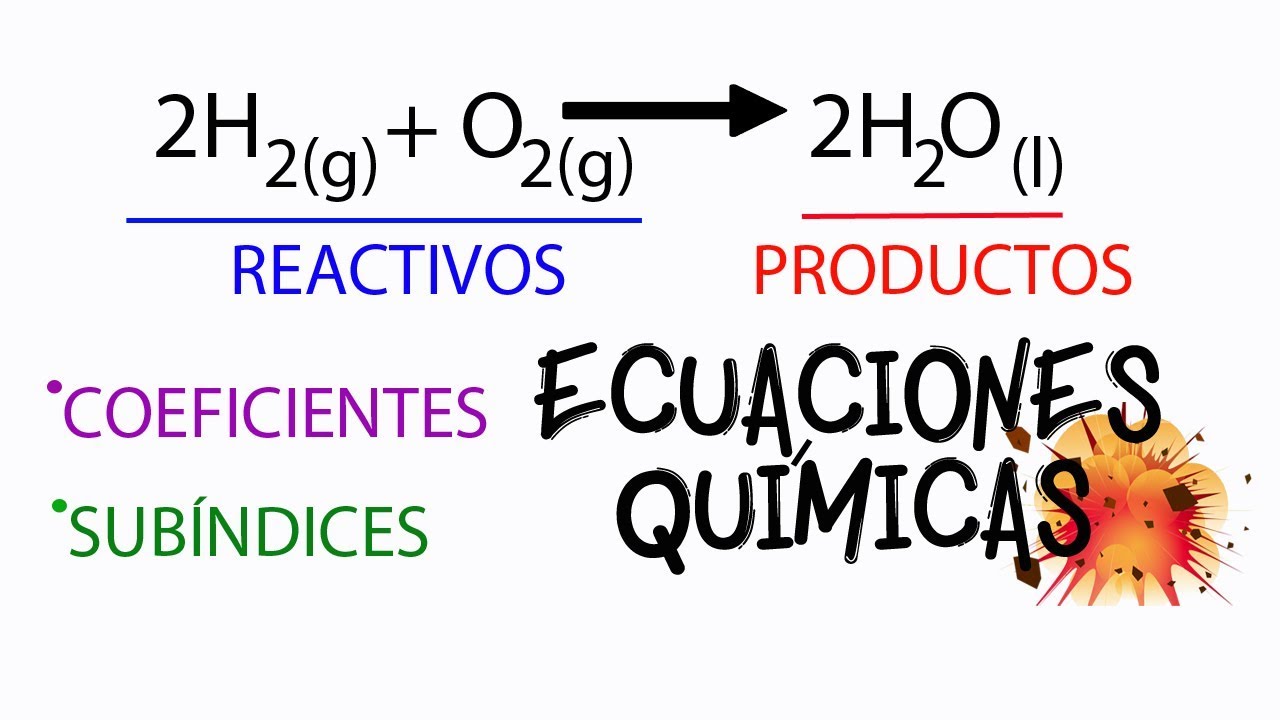
¿Qué son los coeficientes de una reacción química?
Cuando se estudian las reacciones químicas, es común encontrarse con términos como reactantes, productos, ecuaciones químicas, entre otros. Sin embargo, dentro de estos conceptos, los coeficientes de reacción desempeñan un papel muy importante.
Un coeficiente de reacción es un número entero que se coloca delante de una fórmula química para indicar el número de moléculas o átomos que participan en una reacción. Estos coeficientes son cruciales para garantizar que se cumpla la Ley de la Conservación de la Masa, que establece que la masa total de los reactantes debe ser igual a la masa total de los productos.
¿Cómo se determinan los coeficientes de una reacción química?
Para determinar los coeficientes de una reacción química, es necesario utilizar el balanceo de ecuaciones. El balanceo de ecuaciones químicas es el proceso mediante el cual se ajustan los coeficientes de las fórmulas químicas para que haya un equilibrio entre los átomos de los elementos en los reactantes y los productos.
Este proceso se lleva a cabo teniendo en cuenta la Ley de la Conservación de la Masa. Es decir, se debe asegurar que la cantidad de cada elemento en los reactantes sea igual a la cantidad en los productos.
Paso 1: Identificar los elementos
El primer paso para balancear una ecuación química es identificar los elementos que participan en la reacción. Esto se hace observando las fórmulas químicas de los reactantes y los productos.
Por ejemplo:
Si se tiene la siguiente ecuación química:
Fe + O2 → Fe2O3
Los elementos presentes en esta ecuación son el hierro (Fe) y el oxígeno (O).
Paso 2: Contar los átomos
Una vez que se han identificado los elementos presentes en la ecuación, se deben contar los átomos de cada elemento tanto en los reactantes como en los productos.
Por ejemplo:
Para la ecuación anterior, se tiene:
En los reactantes:
– 1 átomo de Fe
– 2 átomos de O
En los productos:
– 2 átomos de Fe
– 3 átomos de O
Paso 3: Balancear los átomos
Una vez que se han contado los átomos de cada elemento en los reactantes y productos, se procede a balancear la ecuación ajustando los coeficientes de las fórmulas químicas.
Por ejemplo:
Siguiendo con el ejemplo anterior, se puede observar que hay más átomos de oxígeno en los productos que en los reactantes. Por lo tanto, se necesita agregar un coeficiente delante de la fórmula del Fe para equilibrar la ecuación.
La ecuación balanceada quedaría de la siguiente manera:
4Fe + 3O2 → 2Fe2O3
Ahora, se puede observar que tanto en los reactantes como en los productos hay:
– 4 átomos de Fe
– 6 átomos de O
Por lo tanto, la ecuación está balanceada y se cumple la Ley de la Conservación de la Masa.
Importancia de los coeficientes de reacción
Los coeficientes de reacción son esenciales para comprender y estudiar las reacciones químicas. Estos nos brindan información sobre la cantidad relativa de átomos o moléculas que intervienen en una reacción, lo que nos permite calcular las cantidades de reactantes necesarias o los productos obtenidos.
Además, los coeficientes de reacción también nos permiten establecer relaciones estequiométricas, es decir, las proporciones en las que los elementos reaccionan entre sí. Estas relaciones se pueden utilizar para determinar la cantidad de un reactante que se necesita para obtener cierta cantidad de un producto, o viceversa.
En resumen, los coeficientes de reacción son indispensables para el estudio de las reacciones químicas, ya que nos ayudan a entender cómo se combinan los elementos y cómo se conserva la masa durante una reacción.
¿Qué sucede si no se balancea una ecuación química?
Si una ecuación química no está balanceada, esto significa que no se cumple la Ley de la Conservación de la Masa. En otras palabras, la cantidad de átomos en los reactantes no es igual a la cantidad de átomos en los productos. Esto puede llevar a resultados incorrectos al realizar cálculos estequiométricos y dificultar el entendimiento de la reacción química en sí.
¿Cuántos coeficientes de reacción se pueden ajustar en una ecuación química?
En teoría, todos los coeficientes de reacción de una ecuación química se pueden ajustar para balancearla adecuadamente. Sin embargo, en la práctica, generalmente se busca la menor cantidad de coeficientes diferentes posible para simplificar la ecuación.
¿Es posible tener un coeficiente de reacción fraccionario?
No. Los coeficientes de reacción siempre deben ser números enteros para representar la cantidad de átomos o moléculas que participan en la reacción. Si se obtiene un coeficiente fraccionario al balancear una ecuación química, estos se deben multiplicar por un número entero para obtener coeficientes enteros.