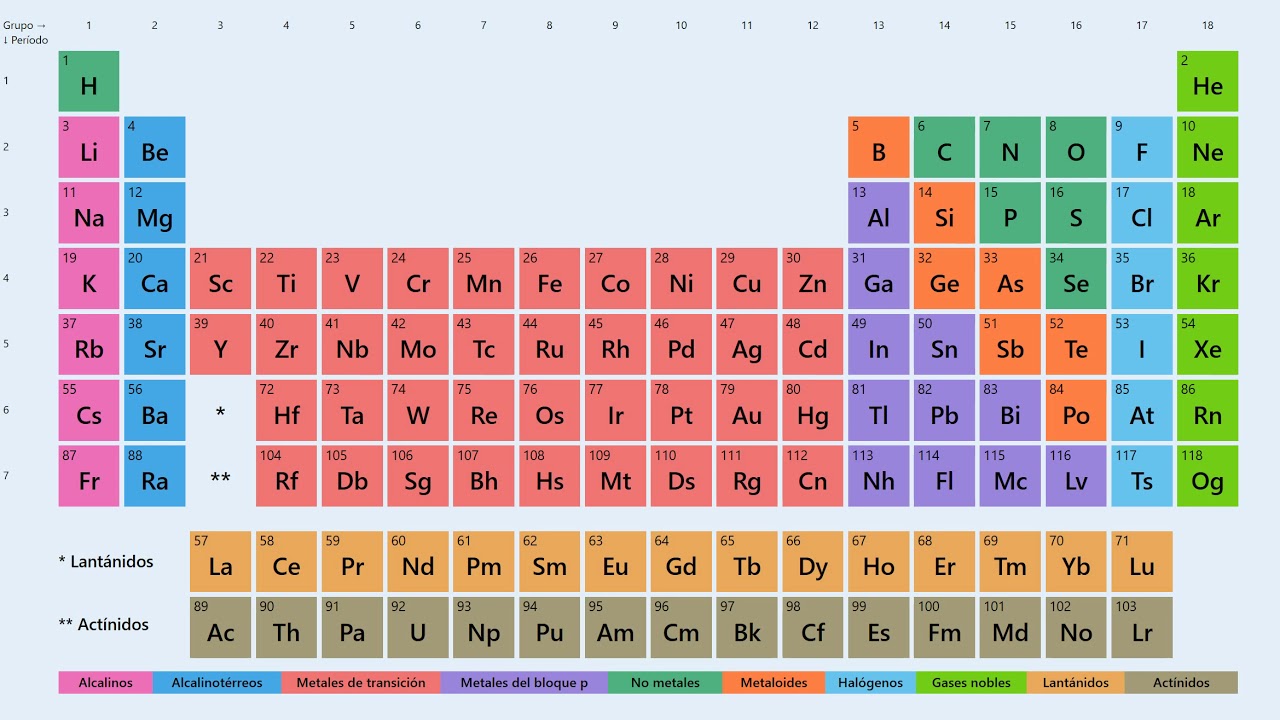
¿Qué son los nombres de las filas de la tabla periódica?
Las filas de la tabla periódica, también conocidas como periodos, son una parte fundamental de la organización de los elementos químicos. Cada fila representa un nivel de energía y se identifica con un número que va del 1 al 7. Sin embargo, en lugar de utilizar estos números, las filas de la tabla periódica se conocen más comúnmente por sus nombres. Estos nombres tienen su origen en los científicos y descubridores de elementos que han realizado aportes significativos a la química.
Período 1: El período de los pioneros
El primer período de la tabla periódica se conoce como el período de los pioneros. Está compuesto por dos elementos, el hidrógeno (H) y el helio (He). El hidrógeno, el elemento más ligero del universo, fue descubierto por Henry Cavendish en 1766. Por otro lado, el helio fue descubierto por Pierre-Jules-César Janssen y Joseph Norman Lockyer en 1868 durante un eclipse solar. Su nombre proviene del griego «helios», que significa sol, ya que fue encontrado en el espectro solar.
Período 2: El período de los alcalinotérreos
El segundo período de la tabla periódica se conoce como el período de los alcalinotérreos. Está compuesto por los elementos berilio (Be), magnesio (Mg), calcio (Ca), estroncio (Sr), bario (Ba) y radio (Ra). Estos elementos tienen propiedades similares y se encuentran en la segunda columna de la tabla periódica. El nombre de este período hace referencia a su similitud con los elementos alcalinos (grupo 1) y los metales de transición (grupo 2).
Período 3: El período del escándalo
El tercer período de la tabla periódica se conoce como el período del escándalo debido a la disputa sobre el descubrimiento y nombre del elemento 43. Este período está compuesto por los elementos sodio (Na), magnesio (Mg), aluminio (Al), silicio (Si), fósforo (P), azufre (S), cloro (Cl), argón (Ar), potasio (K), calcio (Ca) y escandio (Sc). El elemento 43, inicialmente llamado masurio por Carl Auer von Welsbach, fue renombrado tecnecio por Emilio Segrè y Carlo Perrier en 1937 para evitar controversias.
Período 4: El período de la versatilidad
El cuarto período de la tabla periódica se conoce como el período de la versatilidad debido a la variedad de elementos presentes. Está compuesto por los elementos titanio (Ti), vanadio (V), cromo (Cr), manganeso (Mn), hierro (Fe), cobalto (Co), níquel (Ni), cobre (Cu), zinc (Zn), galio (Ga) y germanio (Ge). Estos elementos tienen una amplia gama de aplicaciones en la industria, desde la construcción hasta la electrónica.
Período 5: El período del dolor
El quinto período de la tabla periódica se conoce como el período del dolor debido al proceso de descubrimiento y producción de elementos transuránicos. Está compuesto por los elementos arsénico (As), selenio (Se), bromo (Br), criptón (Kr), rubidio (Rb), estroncio (Sr), itrio (Y), circonio (Zr), niobio (Nb), molibdeno (Mo), tecnecio (Tc), rutenio (Ru), rodio (Rh) y paladio (Pd). Estos elementos tienen diversas aplicaciones en áreas como la medicina, la energía nuclear y la industria química.
Período 6: El período de los lantánidos y actínidos
El sexto período de la tabla periódica se conoce como el período de los lantánidos y actínidos. Está compuesto por los elementos actinio (Ac), torio (Th), protactinio (Pa), uranio (U), neptunio (Np), plutonio (Pu), americio (Am), curio (Cm), berkelio (Bk), californio (Cf), einstenio (Es), fermio (Fm), mendelevio (Md), nobelio (No), laurencio (Lr) y los lantánidos (cerio, praseodimio, neodimio, prometio, samario, europio, gadolinio, terbio, disprosio, holmio, erbio, tulio, iterbio y lutecio). Estos elementos son conocidos por su radioactividad y se utilizan en investigaciones científicas y aplicaciones nucleares.
Período 7: El período de las mechas cortas
El séptimo período de la tabla periódica se conoce como el período de las mechas cortas debido a la brevedad de las filas que lo componen. Está compuesto por los elementos francio (Fr), radio (Ra), actinio (Ac), ametrino (Am), einsteinio (Es), ferrito (Fe), laringio (Lr) y menor (Me). Aunque estos elementos son extremadamente inestables y radioactivos, su estudio es de gran importancia para comprender la física nuclear y la estructura de los átomos.
Los nombres de las filas de la tabla periódica nos permiten tener una forma más fácil de identificar y referirnos a cada período. Desde los pioneros hasta las mechas cortas, cada nombre tiene su propia historia y significado. Estos nombres resaltan la importancia de las contribuciones de los científicos en la química y fortalecen nuestra comprensión de los elementos químicos y su organización en la tabla periódica.
¿Cuántos elementos hay en cada período de la tabla periódica?
Cada período de la tabla periódica está compuesto por un número variable de elementos. Por ejemplo, el primer período solo contiene dos elementos: hidrógeno y helio, mientras que el sexto período tiene 32 elementos, incluyendo los lantánidos y actínidos.
¿Por qué algunos elementos tienen nombres basados en la región donde se descubrieron?
Algunos elementos de la tabla periódica recibieron nombres basados en la región o país donde fueron descubiertos. Por ejemplo, el elemento americio fue nombrado en honor a América debido a que fue descubierto en los Estados Unidos. Esta práctica de nombrar elementos basándose en su lugar de descubrimiento es común y permite reconocer las contribuciones de diferentes regiones al campo de la química.
¿Cuál es la importancia de los nombres de las filas de la tabla periódica?
Los nombres de las filas de la tabla periódica son importantes porque nos brindan una forma más fácil de identificar y referirnos a cada período. Además, estos nombres resaltan las contribuciones de científicos y descubridores de elementos en el campo de la química. Conocer los nombres de las filas de la tabla periódica nos ayuda a comprender mejor la organización de los elementos y su relación en función de propiedades químicas y físicas.